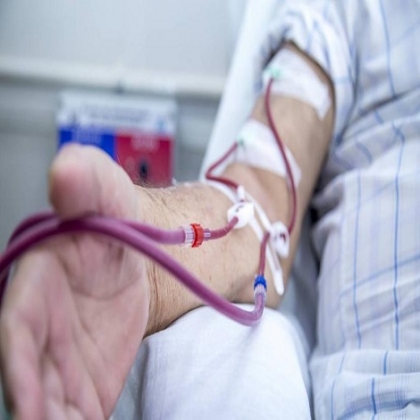
El tratamiento con plasma de pacientes recuperados de Covid-19 a aquellos que padecen la enfermedad de forma grave reporta buenos resultados alrededor del mundo, siendo el Hospital Houston Methodist el primer centro médico académico en implementarlo, desde el 28 de marzo.
El Dr. James M. Musser, jefe del Departamento de Patología y Medicina Genómica del Hospital Houston Methodist, explicó en entrevista con Novedades Yucatán que si bien los científicos médicos de todo el mundo trabajan en las pruebas de nuevos medicamentos y tratamientos contra el Covid-19, la terapia con suero convaleciente, que ya se está implementando de manera experimental en México, emerge como una de las estrategias médicas más prometedoras.
“Al no tener aún cura o tratamientos efectivos comprobados contra el virus, tuvimos que actuar de manera rápida y probar esta terapia. Los primeros resultados con la aplicación de la terapia de plasma convaleciente en pacientes con Covid-19 demostraron que 19 de 25 mejoraron tras recibir las transfusiones provenientes de personas recuperadas del virus, y 11 fueron ya dados de alta”, enfatizó el especialista.
Agregó que sin efectos secundarios adversos encontrados, el estudio concluyó que la transfusión de plasma convaleciente es una opción segura para pacientes con síntomas graves de Covid-19.
Hasta la fecha, y a escala global, éste ha sido el estudio más grande que se ha llevado a cabo para evaluar los resultados relacionados de esta terapia.
“Los anticuerpos de una persona recuperada de Covid-19 están en su máximo nivel entre tres y media a cuatro semanas de que se hace el diagnóstico inicial más dos semanas adicionales en las que la persona recuperada ya no presenta ningún síntoma de la infección”, expuso.
El Dr. Musser detalló que para el uso inicial de esta terapia, los pacientes fueron tratados bajo los lineamientos de emergencia de la Agencia de Medicamentos y Alimentación de los Estados Unidos (la FDA por sus siglas en inglés).
Posteriormente, la FDA aprobó el 3 de abril que más pacientes fueran tratados con la transfusión de plasma.
“Esta aprobación fue extraordinariamente rápida por parte de la FDA, abrió el acceso al tratamiento de plasma convaleciente para pacientes con Covid-19”, apuntó.
Origen del tratamiento
Acerca del origen de la terapia con plasma, el especialista en Medicina Genómica indicó que surgió durante la pandemia de gripe española, hace más de 100 años, en 1918.
“Se utilizó con cierto éxito durante la pandemia del SARS en 2003, la pandemia de influenza AH1N1 en 2009 y el brote de ébola en África de 2015. Después de que muchos pacientes en China mostraron mejoría con esta terapia en un estudio temprano realizado en ese país durante el inicio de la pandemia del Covid-19, un equipo multidisciplinario de científicos médicos del Hospital Houston Methodist apuntó rápidamente a comenzar a combatir el nuevo coronavirus con la terapia de suero convaleciente”, mencionó el experto en patología.
Agregó que debido a la urgencia de encontrar tratamientos efectivos, se publicó un informe preliminar en el servidor médico de consulta medRxiv, que aún no ha sido revisado por otros investigadores colegas médicos.
El manuscrito se titula “Tratamiento de plasma convaleciente para pacientes con COVID-19 en Houston, Texas”.
Dicho informe se envió para su revisión a una destacada revista médica, aunque no se trate aún de la versión final.
El doctor Musser es el autor del estudio. Por su parte, el Doctor Eric Salazar, profesor asistente de Patología y Medicina Genómica del Instituto de Investigación del Hospital Houston Methodist, es el investigador principal que dirigió el proyecto para tratar a pacientes críticos con Covid-19 mediante plasma convaleciente de personas recuperadas.
El entrevistado también mencionó que estos resultados fueron muy similares a los obtenidos recientemente en el estudio de uso compasivo del antiviral Remdesivir para ayudar a tratar el Covid-19.